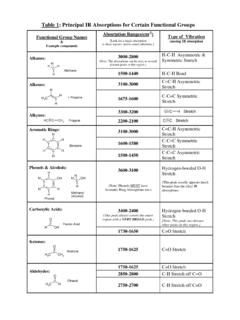
Transcription of Résumé de cours : Spectres Infrarouge - ticedu.fr
1 R sum de cours : Spectres Infrarouge I. Introduction : Le rayonnement Infrarouge (IR), invisible l il nu, est situ dans domaine de longueur d onde sup rieur 800 nm. Lorsqu un chantillon est travers par un faisceau lumineux IR, une partie de la lumi re est absorb e. C est gr ce cette absorption que nous allons pouvoir d celer la pr sence de groupements d atomes caract ristiques. Les mol cules, au passage du rayonnement IR, subissent des mouvements de vibration internes (d' longation et de d formation). Ces vibrations sont l origine des pics et des bandes d absorption que nous observons sur le spectre du parac tamol ci-dessous : II. Pr sentation d spectre IR En ordonn e, la transmittance en %, qui repr sente le pourcentage de lumi re ayant travers l chantillon.
2 En abscisse, le nombre d onde (l inverse de la longueur d onde) en cm-1 Il existe deux zones principales dans un spectre IR : Une premi re zone gauche correspondant un nombre d onde sup rieur 1400 cm-1 o se trouvent les bandes caract ristiques des liaisons de la mol cule Une seconde zone droite correspondant un nombre d onde inf rieur 1400 cm-1, appel e empreinte digitale que nous ne pourrons pas analyser cause de sa complexit . 3. Les groupes fonctionnels Les groupements d atomes (appel s aussi groupes fonctionnels) les plus courants et d tectables par spectre IR sont : - Les alcools - Les acides carboxyliques - Les ald hydes - Les c tones - Les esters - Les amines - Les amides Au-del de la d tection de ces groupes, il est difficile d obtenir suffisamment d informations d un spectre IR pour pouvoir en d duire l int gralit de la structure de la mol cule.
3 En savoir plus sur les groupes fonctionnels : T l charger l application sp cifiquement con ue pour apprendre les groupes fonctionnels Mirage groupes fonctionnels sur Android/iOS. IV. Lecture du spectre : Afin d identifier les groupes fonctionnels pr sents dans une mol cule, on dispose de tables suivantes : V. La liaison hydrog ne : La liaison hydrog ne est une interaction d origine lectrique entre mol cules. Sans liaison hydrog ne, il n y a par exemple pas d eau l tat solide ou liquide. A cause des lectron gativit s diff rentes des atomes composant la mol cule d eau (H20), il y a aura un surplus d lectrons au niveau de l atome d oxyg ne (le plus lectron gatif) et un d ficit Fonction liaison Nombre d onde intensit Alcool O-H alcool libre De 3580 3670 Forte (fin) O-H alcool li De 3200 3400 Forte (large) Acide carboxylique O-H alcool li De 3200 3400 Forte (large)
4 C=O acide De 1680 1720 Forte Ald hyde Ctrigonal-H ald hyde De 2750 2900 Moyenne C=O ald hyde De 1650 1730 Forte Amide C=O De 1650 1700 Forte N-H amide De 3100 3500 Moyenne N-H amide De 1560 1640 Forte / Moyenne Amine N-H amine De 3100 3500 Moyenne N-H amine De 1560 1640 Forte / Moyenne Anhydrides C=O 1760 et 1810 2 absorptions Ester C=O ester De 1700 1750 Forte C-O ester 1000 et 1300 2 absorptions C tone C=O c tone De 1650 1730 Forte d lectrons au niveau des deux atomes d hydrog ne (les moins lectron gatifs). Le pourcentage de transmittance du spectre IR et la forme des bandes d absorption va tre modifi par la pr sence de cette liaison hydrog ne. VI. OH libre : l' tat gazeux, une bande d' absorption forte et fine vers 3620cm-1est caract ristique de liaison O-H.
5 Il n'existe pas, dans cet tat physique, de liaison hydrog ne entre les mol cules d' thanol, la liaison O-H est appel e O-H libre . Le m me comportement sera observ lorsque l alcool est tr s dilu . VII. OH li : l' tat liquide, une bande d' absorption forte et large de 3200cm-1 3400cm-1est caract ristique de la liaison O-H. Les liaisons hydrog ne tablies entre les mol cules d'alcool affaiblissent les liaisons O-H. Cela implique alors un largissement de la band. La liaison O-H est dans ce cas dite O-H li e . VIII. Ce qu il faut retenir Si le groupe carbonyle est pr sent : Ald hyde : Chercher la pr sence de la liaison C-H entre 2750 et 2900 cm-1 Ester : Chercher dans la partie d empreinte digitale le groupement C-O entre 1000 et 1300 cm-1 Acide : Chercher une bande large caract ristique du groupement O-H entre 3200 et 3400 cm-1 Amides : Chercher la pr sence de deux bandes N-H dans la bande 3500 cm-1 (intensit moyenne forte) Anhydrides : Chercher 2 absorptions C=O 1760 et 1810 cm-1 C tone : Si aucune autre absorption caract ristique Si le groupe carbonyle n est pas pr sent : Alcools : Chercher une bande large caract ristique du groupement O-H entre 3200 et 3400 cm-1 (Attention l tat physique) Amines.
6 Chercher la pr sence de deux bandes N-H dans la bande 3500 cm-1