ALLEGATO I RIASSUNTO DELLE CARATTERISTICHE DEL …
trattamento con oclacitinib (secondo il regime di somministrazione raccomandato) non è chiara. 4.9 Posologia e via di somministrazione Per uso orale. Dosaggio e schema di trattamento: La dose iniziale raccomandata di oclacitinib è di 0,4-0,6 mg/kg peso corporeo, somministrata per via orale, due volte al giorno fino a 14 giorni.
Tags:
Somministrazione, Di somministrazione
Information
Domain:
Source:
Link to this page:
Please notify us if you found a problem with this document:
Documents from same domain
Q12 Step 2b Technical and regulatory …
www.ema.europa.euICH guideline Q12 on technical and regulatory considerations for pharmaceutical product lifecycle management EMA/CHMP/ICH/804273/2017 Page 3/36
Product, Management, Lifecycle, Product lifecycle management
Guideline on good pharmacovigilance practices …
www.ema.europa.eu9 December 2013 . EMA/816292/2011 Rev 1* Guideline on good pharmacovigilance practices (GVP) Module VII – Periodic safety update report (Rev 1)
Guidelines, Good, Practices, Guideline on good pharmacovigilance practices, Pharmacovigilance
Guideline on good pharmacovigilance practices (GVP)
www.ema.europa.euGuideline on good pharmacovigilance practices (GVP) – Module IX (Rev 1) EMA/827661/2011 Rev 1 Page 2/25
Guideline on good pharmacovigilance practices …
www.ema.europa.euGuideline on good pharmacovigilance practices (GVP) – Module VIII (Rev 3) EMA/813938/2011 Rev 3 Page 2/28
Guidelines, Good, Practices, Guideline on good pharmacovigilance practices, Pharmacovigilance
Guideline for good clinical practice E6(R2)
www.ema.europa.euGuideline for good clinical practice E6(R2) EMA/CHMP/ICH/135/1995 Page 2/70 Document History First Codification History Date New Codification
Guideline for good clinical practice E6(R2)
www.ema.europa.euGuideline for good clinical practice E6(R2) EMA/CHMP/ICH/135/1995 Page 2/75 10 Document History 11 First Codification History Date New Codification November
Guidelines, Good, Practices, Clinical, Good clinical practice e6
Guideline on good pharmacovigilance practices …
www.ema.europa.euharmful physical or psychological effects [DIR 2001/83/EC Art 1(1 6)]. 74 Adverse event (AE); synonym: Adverse experience 75 Any untoward medical occurrence in a patient or clinical- trial subject administered a medicinal product
Guidelines, Good, Practices, Guideline on good pharmacovigilance practices, Pharmacovigilance
European Medicines Agency
www.ema.europa.eu© EMEA 2006 2 SPECIFICATIONS: TEST PROCEDURES AND ACCEPTANCE CRITERIA FOR BIOTECHNOLOGICAL/BIOLOGICAL PRODUCTS ICH Harmonised Tripartite Guideline
Guidelines, European, Agency, Medicine, Harmonised, European medicines agency, Ich harmonised
products1/traditional herbal medicinal products
www.ema.europa.euThere is no expectation that existing herbal medicinal products on the market will be affected by this guideline, with the exception of traditional herbal medicinal products for human use that were already
Product, Medicinal, Traditional, Herbal, Products1 traditional herbal medicinal products, Products1
Q7 Q&A - good manufacturing practice for active ...
www.ema.europa.euICH guideline Q7 on good manufacturing practice for active pharmaceutical ingredients – questions and answers EMA/CHMP/ICH/468930/2015 Page 2/37
Good, Practices, Pharmaceutical, Manufacturing, Active, Ingredients, Good manufacturing practice for active, Good manufacturing practice for active pharmaceutical ingredients
Related documents
Reazioni di ipersensibilità - Unife
www.unife.italimenti confezionati •Oltre 120 alimenti sono stati descritti come ... somministrazione rapida di adrenalina. Prick test •Consiste nell’inoculo sotto cute della sostanza da testare •L’eventuale reazione infiammatoria si ... povero di cellule e di O 2. Complesso primario
CODICE INTERNAZIONALE RACCOMANDATO DI PRATICHE …
www.salute.gov.itsomministrazione degli alimenti e consumatori, ha la responsabilità di garantire che l’alimento sia sicuro e adatto al consumo. Questi principi generali sono una solida base per garantire l'igiene alimentare e dovrebbero essere abbinati
Scheda 5.2 – Autorizzazione sanitaria (sostanze alimentari)
www.tuttocamere.itAutorizzazione sanitaria relativa alla produzione, preparazione, confezionamento, somministrazione e deposito di alimenti e bevande Le suddette attività necessitano, ai sensi dell'art. 2 della L. 283/62, dell'autorizzazione sanitaria rilasciata
Alimenti, Sanitaria, Autorizzazione, Sostanze, Somministrazione, Alimentari, Somministrazione e, Autorizzazione sanitaria, Sostanze alimentari, Di alimenti e
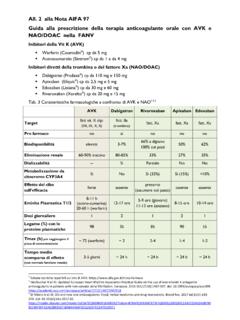
All. 2 alla Nota AIFA 97 Guida alla prescrizione della ...
www.aifa.gov.itDosaggi, modalità di somministrazione e follow-up Dosaggi Le dosi sono personalizzate in rapporto al valore di INR, che nella FANV deve essere mantenuto in un range fra 2 e 3. Modalità di somministrazione: Sia per warfarin che per acenocumarolo è prevista la monosomministrazione quotidiana, preferibilmente lontano dai pasti.
Somministrazione, Di somministrazione, Di somministrazione e
11 reazioni a rapida insorgenza - FIMMG
torino.fimmg.orgLe reazioni che si possono osservare dopo la somministrazione di un vaccino e che necessitano di essere adeguatamente valutate ed eventualmente trattate possono essere così classificate (2)(6): 1. Spasmi respiratori (affettivi o di singhiozzo) 2. Crisi d’ansia 3. Svenimento - collasso 4. Episodio di ipotonia -iporesponsività (HHE) 5.
Cosa devi sapere dopo il vaccino Johnson & Johnson/Janssen ...
www1.nyc.govPrima di lasciare il centro di vaccinazione: Assicurati di ricevere una scheda di vaccinazione con il nome del vaccino fatto e la data di somministrazione. Fanne una fotografia o una copia e conserva l’originale in un posto sicuro. Devo ritornare per una seconda dose del vaccino? No. Il vaccino Johnson & Johnson richiede una sola dose.